| La société allemande modag a annoncé au mois de juillet avoir levé 12 millions d'euros pour développer un médicament pour l’atrophie multisystématisée appelé Anle138b. Dans l'article d'aujourd'hui, je vous propose de revoir pourquoi cette nouvelle est importante pour la communauté des malades de Parkinson . Nous discuterons du mode d’action de la molécule Anle138b, de ce qu’est l’atrophie multisystématisée, et de ses liens avec la maladie de Parkinson. |
Le mois dernier, une petite entreprise de biotechnologie allemande appelé MODAG est sortie de son "mode furtif ». Dans le développement des start-up, le mode furtif est l’état temporaire de secret complet qu’une entreprise s’impose, généralement mis en place pour éviter d’alerter ses concurrents du lancement imminent d’un produit.
Après des années de développement d'un nouveau médicament, la société allemande est donc sortie du mode furtif en levant 12 millions d'euros de financement de série A, qui seront utilisée pour tester cliniquement son nouveau traitement appelé Anle138b.
 Le test prévu est un essai clinique de phase I (qui est un test de sécutrité réalisé sur des individus en bonne santé), mais les phases suivantes porteront ensuite leur attention sur des individus présentant une atrophie multisystématisée.
Le test prévu est un essai clinique de phase I (qui est un test de sécutrité réalisé sur des individus en bonne santé), mais les phases suivantes porteront ensuite leur attention sur des individus présentant une atrophie multisystématisée.Qu'est-ce que l'atrophie multisystématisée?
L'atrophie multisystématisée (ou MSA suivant son acronyme anglais) également appelée syndrome de Shy-Drager est une affection neurodégénérative rare.
Elle est considéré comme un parkinsonisme atypique.
Qu'est-ce qu'un «parkinsonisme atypique»?
Le «parkinsonisme» fait référence à un large groupe d’affections neurologiques à l’origine des caractéristiques de mouvement similaires à celles observées dans la «maladie de Parkinson», telles que tremblements, mouvements lents et raideurs. Le terme «parkinsonisme» est souvent utilisé comme terme générique qui recouvre la «maladie de Parkinson» et tous les autres «parkinsonismes».
Les parkinsonismes sont généralement divisés en trois groupes:
- Parkinson classique idiopathique (forme spontanée courante de la maladie appelée «maladie de Parkinson»)
- Syndromes de Parkinson ou Parkinson-plus atypiques (tels que l’atrophie multisystématisée et la paralysie supranucléaire progressive (PSP))
- Parkinson secondaire (pouvant être provoqué par des mini-accidents vasculaires cérébraux, médicaments, traumatismes crâniens, etc.)
 Source: Parkinsonspt
Source: ParkinsonsptQuelle est donc la différence entre l’atrophie multisystématisée et la maladie de Parkinson idiopathique?
Quand une personne se présente pour la première fois à l’examen clinique avec une rigidité, une lenteur de mouvement et un tremblement de repos, il peut être très difficile de faire la différence entre le Parkinson idiopathique classique et d’autres types de parkinsonismes. Cependant, certains signes révélateurs peuvent aider à différencier l’atrophie multisystématisée de la maladie de Parkinson idiopathique:
Le handicap progresse plus rapidement dans la MSA
Les personnes atteintes de MSA répondent peu au traitement au lévodopa au fil du temps
La rétention urinaire et l'hypotension orthostatique (la pression artérielle baisse lorsque vous vous levez soudainement) sont courantes
La rigidité et la bradykinésie sont hors de proportion avec les tremblements
La parole est gravement touchée
Respiration sifflante et forte respiration sifflante lorsque la respiration sont présents
Dans la grande majorité des cas, il n’ya pas de démence, bien que d’autres fonctions cognitives puissent être affectées.
Réduction des yeux clignotants et de la sécheresse oculaire, en plus des mouvements oculaires saccadés ou plus lents
Il convient de noter que la présence d’un ou deux de ces signes n’indique pas nécessairement qu’un individu est atteint de MSA.
Existe-t-il différents types de MSA?
La deuxième déclaration consensuelle sur le diagnostic de l'atrophie multisystématisée prévoit deux types fondamentaux d'atrophie multisystématisée, basés sur les symptômes de la maladie au moment de l'évaluation.
Ces deux types sont:
- MSA avec parkinsonisme prédominant (MSA-P), qui peut ressembler à un Parkinson idiopathique en raison de la lenteur de ses mouvements et de ses muscles raides. Les termes dégénérescence striatonigrale ou variante parkinsonienne sont parfois utilisés pour cette catégorie de MSA.
- MSA avec traits cérébelleux (MSA-C). On l’appelle parfois «atrophie olivopontocérébelleuse sporadique» (ou OPCA). MSA-C affecte principalement l'équilibre, la coordination et la parole.
Certains chercheurs pensent qu’il existe également un troisième type de MSA, qui serait une combinaison des deux.
Comment diagnostique-t-on l'atrophie multisystématisée?
À l'heure actuelle, aucun test ne peut établir ou confirmer définitivement le diagnostic de MSA chez une personne vivante.
Cela dit, l’utilisation régulière de techniques d’imagerie cérébrale telles que l’IRM et la tomodensitométrie peut indiquer une diminution de la taille des structures cérébrales spécifiques affectées par le MSA (comme le cervelet et le pons). Par exemple, dans l'image ci-dessous, vous pouvez voir des images IRM en série du cerveau d'une personne atteinte de MSA-C sur une période de 2 ans. Notez la réduction subtile de la taille de la forme caractéristique de «croix» des ponts entre l’image C (2004) et deux ans plus tard dans l’image D (2006):
IRM en série du cerveau d'une personne atteinte de MSA-C sur une période de 2 ans. Source: Openi
Et dans les images IRM du cerveau analysées chez des personnes atteintes de MSA-P, il se produit un assombrissement progressif de la région du cerveau appelée putamen (indiquée sur le côté gauche du cerveau par une flèche blanche dans l'image ci-dessous). Vous pouvez constater qu'au fil du temps, au fur et à mesure que la maladie progresse (de la classe 0 à la classe 3), le putamen devient de plus en plus sombre.
 evolution avec le temps de l'IRM du cerveau d'une personne atteinte de MSA-P Source: e-jmd
evolution avec le temps de l'IRM du cerveau d'une personne atteinte de MSA-P Source: e-jmdQu'est-ce qui cause l'atrophie multisystématisée?
Je pense que la plupart des chercheurs conviendraient que la bonne réponse à cette question est:
Source: Wellbeing365
Mais de nombreux chercheurs pensent que le développement de la MSA est associé à l’agrégation de la protéine associée à la maladie de Parkinson, l’alpha synucléine.
Rappelez-moi une fois de plus qu'est-ce que l'alpha synucléine?
L’alpha-synucléine est l’une des protéines les plus répandues dans notre cerveau. Elle représente environ 1% de toutes les protéines d'un neurone. Lorsque la protéine alpha-synucléine est produite par une cellule, elle est normalement appelée «protéine non repliée», en ce sens qu’elle n’a pas réellement de structure définie.
Lorsqu’elle est produite, l’alpha synucléine ressemble initialement à ceci:
Alpha synucleine. Source: Wikipedia
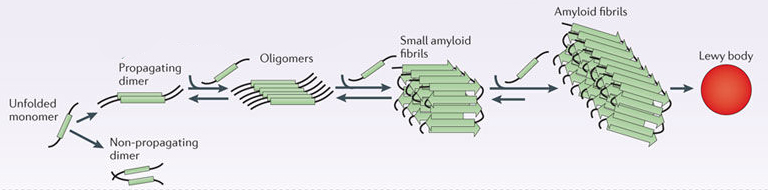
Sous cette forme, l'alpha synucléine est considérée comme un monomère - qui est une molécule unique pouvant se lier à d'autres molécules. Lorsqu'elles se lient à d'autres protéines d'alpha synucléine, elles forment un oligomère (une collection d'un certain nombre de monomères dans une structure spécifique). On pense que l'alpha synucléine a certaines fonctions en tant que monomère, mais peut également avoir des tâches spécifiques en tant qu'oligomère.
Dans la maladie de Parkinson, l’alpha synucléine se plie également et s’agrège pour former des fibrilles amyloïdes.

Images microscopiques de monomères, d'oligomères et de fibrilles. Source: Brain
Et on pense que les formes d'oligomère et de fibrilles de la protéine alpha-synucléine s'agrègent, puis forment ce que nous appelons des corps de Lewy.
Les corps de Lewy sont des inclusion cellulaire, ils se trouvent presque toujours à l'intérieur du corps cellulaire des neurones. Ils sont une caractéristique du cerveau parkinsonien.
Une photo d'un corps de Lewy à l'intérieur d'un neurone. Source: Neuropathology-web
Mais je pensais que l’alpha synucléine était associée à la maladie de Parkinson?
C’est vrai, mais certaines recherches suggèrent que différents variétés d’apha synucléine pourraient influencer les deux maladies (Cliquez ici pour en savoir plus à ce sujet).
Donc, MODAG va tester son médicament (Anle138b) pour la MSA?
Oui.
Et que fait Anle138b?
Anle138b est un composé diphényl-pyrazole. Ne vous inquiétez pas : c'est juste le nom que l'on donne aux molécules possédant un noyau avec 2 azotes (notés N dans la formule développée) dans un cycle à 5 atomes, sur lequel sont branchés deux phényl (les cycles à 6 carbones de part et d'autre).
Cette molécule possède de puissantes propriétés d’agrégation anti-protéines.
Anle138b. Source: Pubchem

Title: Anle138b: a novel oligomer modulator for disease-modifying therapy of neurodegenerative diseases such as prion and Parkinson’s disease.
Authors: Wagner J, Ryazanov S, Leonov A, Levin J, Shi S, Schmidt F, Prix C, Pan-Montojo F, Bertsch U, Mitteregger-Kretzschmar G, Geissen M, Eiden M, Leidel F, Hirschberger T, Deeg AA, Krauth JJ, Zinth W, Tavan P, Pilger J, Zweckstetter M, Frank T, Bähr M, Weishaupt JH, Uhr M, Urlaub H, Teichmann U, Samwer M, Bötzel K, Groschup M, Kretzschmar H, Griesinger C, Giese A.
Journal: Acta Neuropathol. 2013 Jun;125(6):795-813
PMID: 23604588
(cet article est en OPEN ACCESS si vous souhaitez le lire)
Dans cette première étude, les chercheurs ont découvert Anle138b en réalisant une vaste étude de dépistage visant à identifier des molécules pouvant inhiber la forme toxique de l’alpha synucléine.
Ils ont ensuite testé Anle138b dans des modèles de la maladie de parkinson basés sur des cultures de cellules et de srongeurs et ont découvert qu’il était neuroprotecteur et qu’il inhibait très bien la forme toxique de l’alpha synucléine. Et le traitement semble être très efficace. Dans l'image ci-dessous, vous pouvez voir une coloration sombre de l'alpha synucléine toxique dans le panneau gauche du cerveau d'une souris non traitée, mais très peu dans le panneau droit d'une souris traitée à l'Anle138b.
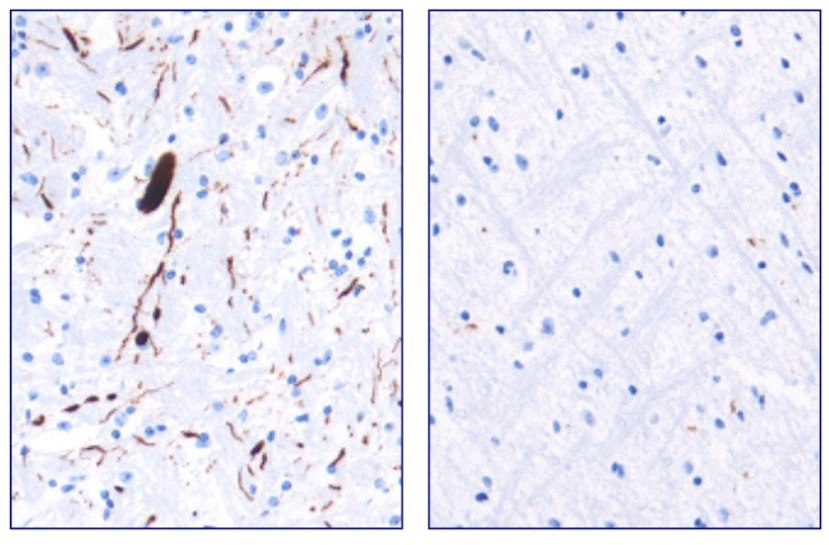
Toxic form of alpha synuclein (dark staining). Source: Max-Planck
Fait important, Anle138b n'interfère pas avec la production et le comportement normal de la protéine alpha synucléine chez la souris, mais agit en tant qu'inhibiteur de l'agrégation de l'alpha synucléine (considérée comme la forme toxique de la protéine). En outre, les chercheurs n'ont constaté aucun effet toxique d'Anle138b dans aucune de leurs expériences, même après un traitement prolongé à haute dose (plus d'un an).
Et dans une étude de suivi, le médicament était efficace même s'il avait été administré après le début de la maladie modèle:

Title: The oligomer modulator anle138b inhibits disease progression in a Parkinson mouse model even with treatment started after disease onset
Authors: Levin J, Schmidt F, Boehm C, Prix C, Bötzel K, Ryazanov S, Leonov A, Griesinger C, Giese A.
Journal: Acta Neuropathol. 2014 May;127(5):779-80.
PMID: 24615514 (This article is OPEN ACCESS if you would like to read it)
Au cours de la première étude, les chercheurs avaient commencé le traitement à Anle138b dans le modèle murin de Parkinson à un très jeune âge. Dans cette étude, toutefois, les chercheurs ont utilisé des souris génétiquement modifiées qui produisent des niveaux élevés d'une version mutante de la protéine alpha synucléine humaine (A30-P) et n'ont commencé le traitement que lorsque les symptômes commençaient à apparaître. Ces souris commencent à présenter des symptômes ressemblant à la maladie de Parkinson à environ 300 jours d’âge. Les chercheurs ont commencé à traiter les souris à l'âge de 350 jours et ont découvert qu'Anle138b améliorait considérablement la survie globale des souris.
Plus récemment, les chercheurs ont poursuivi ces recherches en étudiant Anle138b dans un modèle murin de MSA:

Title: Anle138b modulates α-synuclein oligomerization and prevents motor decline and neurodegeneration in a mouse model of multiple system atrophy.
Authors: Heras-Garvin A, Weckbecker D, Ryazanov S, Leonov A, Griesinger C, Giese A, Wenning GK, Stefanova N.
Journal: Mov Disord. 2019 Feb;34(2):255-263. doi: 10.1002/mds.27562. Epub 2018 Nov 19.
PMID: 30452793
(cet article est également en OPEN ACCESS si vouys souhaitez le lire en détail)
Le modèle de souris PLP-hαSyn récapitule bon nombre des caractéristiques cliniques et physiopathologiques de la MSA, et les chercheurs qui ont mené cette étude ont utilisé ces souris pour tester le potentiel d'Anle138b en tant que traitement contre la MSA. Les chercheurs ont découvert que le traitement des souris pendant 4 mois avec Anle138b réduisait de manière significative l’accumulation de l’alpha synucléine, ce qui entraînait une neuroprotection et une réduction de l’activation du système immunitaire chez les souris (par rapport aux animaux traités avec un placebo). Le traitement Anle138b a également contribué à préserver la fonction motrice chez les souris.
Et ces résultats ont donné à MODAG confiance dans le passage aux essais cliniques d'Anle138b chez l'homme.
Qu'en est-il de la maladie de Parkinson?
Tout récemment, un groupe de recherche de l’université de Cambridge a démontré le potentiel d’Anle138b dans un nouveau modèle murin de Parkinson:
 Title:
Depopulation of dense α-synuclein aggregates is associated with rescue
of dopamine neuron dysfunction and death in a new Parkinson’s disease
model.
Title:
Depopulation of dense α-synuclein aggregates is associated with rescue
of dopamine neuron dysfunction and death in a new Parkinson’s disease
model.Authors: Wegrzynowicz M, Bar-On D, Calo’ L, Anichtchik O, Iovino M, Xia J, Ryazanov S, Leonov A, Giese A, Dalley JW, Griesinger C, Ashery U, Spillantini MG.
Journal: Acta Neuropathol. 2019 May 31. doi: 10.1007/s00401-019-02023-x.
PMID: 31165254
Ces souris ont présenté une réduction progressive des niveaux de dopamine et une mort cellulaire significative de la dopamine à partir de l'âge de 6 et 12 mois, respectivement. Les animaux ont commencé à présenter les premiers signes de troubles moteurs dès l'âge de 9 mois et les problèmes moteurs globaux à 20 mois (50% des neurones dopaminergiques avaient été perdus). Ce modèle de souris semble très bien ressembler à la maladie de parkinson humaine.
De manière remarquable, le traitement avec Anle138b âgé de 9 à 12 mois a restauré les niveaux de dopamine, a empêché la mort des cellules dopaminergiques et a amélioré les déficiences motrices chez les souris. En dépit du traitement tardif, Anle138b était toujours capable d’avoir un effet bénéfique chez ces souris. Cette découverte valide et développe des études antérieures similaires comportant un traitement retardé avec Anle138b (Cliquez ici pour en savoir plus à ce sujet).
Ce dernier projet a été soutenu par le Cure Parkinson's Trust, l'association Parkinson's UK et la Fondation Michael J Fox. Il sera intéressant de voir si, après l’essai clinique de phase I d’Anle138b, ces organisations encouragent MODAG à mener une phase II chez les personnes atteintes de la maladie de Parkinson.
Résumons nous :
La nouvelle selon laquelle la société allemande de biotechnologie MODAG est sortie de son mode furtif et commence actuellement un programme d'essais cliniques pour son composé principal - le médicament anti-agrégation de protéines Anle138b - est très encourageante. Ce composé a été développé avec prudence et la société est maintenant convaincue que Anle138b est prêt pour un essai clinique.
Nous allons surveiller de très près l’évolution du développement clinique de ce médicament et, s’il est démontré que son innocuité est garantie chez l’homme après les essais de phase I, nous serons heureux de voir ce composé testé plus avant dans différents parkinsonismes et de vous tenir informé de ces résultats






Aucun commentaire:
Enregistrer un commentaire